Odeurs fruitées et parfums synthétiques
Les parfums naturels, très chers car difficiles à extraire et à purifier, sont souvent remplacés par des produits chimiques synthétiques moins coûteux, comme par exemple les aldéhydes ou les esters. Dans cette expériences, nous reproduirons quelques odeurs fruitées ou synthétiques par des réactions d'estérification conduisant aux esters.
Sommaire
1 Précautions
Outre les précautions en chimie qui sont d'usage, cette expérience comporte les attentions suivantes :
- Manipuler les acides avec grande précautions, surtout l'acide sulfurique
 . Attention à l'endroit où vous poser les pipettes qui ont été utilisées, les acides sont corrosifs, certains dégagent de très fortes odeurs.
. Attention à l'endroit où vous poser les pipettes qui ont été utilisées, les acides sont corrosifs, certains dégagent de très fortes odeurs. - Les alcools sont des produits nocifs et hautement inflammables
 . Rebouchez soigneusement les flacons et éloignez-les de toutes sources de chaleur, flamme ou lumière.
. Rebouchez soigneusement les flacons et éloignez-les de toutes sources de chaleur, flamme ou lumière. - Le méthanol


 est extrêmement inflammable et mortel en faibles quantités : porter absolument des gants et manipuler sous hotte aspirante.
est extrêmement inflammable et mortel en faibles quantités : porter absolument des gants et manipuler sous hotte aspirante. - Ne respirez pas les parfums directement en sortie du tube après ébullition mais portez l'odeur à votre nez avec la main.
- Les esters obtenus sont totalement impropres à la consommation, ne pas les goûter et ne pas se les mettre sur la peau ! Les esters sont généralement des produits inflammables et irritants

 .
.
2 Matériel
- Tubes à essai
- Pince en bois
- Bec Bunsen
- Pipettes jetables en plastique, pipettes Pasteur ou compte-gouttes
- Spatule
- Acides :
- Alcools :
- Méthanol



- Éthanol

- Alcool isoamylique (3-méthylbutan-1-ol)


- Hexanol

- Linalol


- Alcool benzylique (phénylméthanol)

- 2-phényléthanol


- Méthanol
- Acide sulfurique concentré H2SO4

- Granulés de pierre ponce
3 Protocole expérimental
- Pour chaque odeur, nous utilisons un tube à essai différent. Dans le tube, placer un petit grain de pierre ponce, 4 gouttes d'acide sulfurique concentré à l'aide d'une pipette, et une petite quantité de l'acide et de l'alcool choisis en respectant les mélanges et les quantités indiquées ci-dessous.
| Acide (quantité) | Alcool (quantité) | Ester | Odeur résultante |
|---|---|---|---|
| Acide éthanoïque 10 gouttes | Alcool isoamylique 20 gouttes | Acétate d'isoamyle | Banane |
| Acide éthanoïque 10 gouttes | Éthanol 20 gouttes | Acétate d'éthyle | Dissolvant |
| Acide éthanoïque 10 gouttes | Hexanol 20 gouttes | Acétate d'hexyle | Poire |
| Acide éthanoïque 10 gouttes | Linalol 20 gouttes | Acétate de linalyle | Bergamote |
| Acide éthanoïque 10 gouttes | 2-phényléthanol 20 gouttes | Acétate de 2-phényléthyle | Rose |
| Acide éthanoïque 10 gouttes | Alcool benzylique 20 gouttes | Acétate de benzyle | Jasmin |
| Acide butanoïque* 10 gouttes | Éthanol 8 gouttes | Butanoate d'éthyle | Ananas* |
| Acide butanoïque* 10 gouttes | Alcool benzylique 12 gouttes | Butanoate de benzyle | Non testé* |
| Acide butanoïque* 10 gouttes | Alcool isoamylique 12 gouttes | Butanoate d'isoamyle | Pomme* |
| Acide salicylique 0,1 g | Méthanol 20 gouttes | Salicylate de méthyle | Winter-green, Reine des prés |
| Acide salicylique 0,1 g | Hexanol 20 gouttes | Salicylate d'hexyle | Azalée |
| Acide benzoïque 0,4 g | Éthanol 20 gouttes | Benzoate d'éthyle | Non testé |
| Acide propanoïque* 20 gouttes | Éthanol 15 gouttes | Propanoate d'éthyle | Non testé* |
* L'acide propanoïque et l'acide butanoïque ont une très forte odeur désagréable (entre le rance et le vomit...) ! De fait, si la réaction n'est pas totale, l'odeur fruitée de l'ester peut être masquée par l'odeur de l'acide. Pour cette raison, on évite généralement de réaliser ces esters... Les autres acides listés ici n'ont pas cet inconvénient.

Parmi les non testés, on doit retrouver les parfums : rhum, cerise et fruité.
- Saisir le tube avec la pince en bois puis chauffer doucement le bas du tube à essai au-dessus de la flamme du bec Bunsen de manière uniforme (ne pas chauffer en un seul point du tube).
- Après ébullition durant une minute, porter le tube près de vous et diriger les vapeurs vers votre nez avec la main. Comparer l'odeur obtenue avec les indications du tableau ci-dessus.
- Certaines estérifications demandent un temps de chauffage plus long ; certaines odeurs subtiles peuvent êtres masquées par l'odeur (souvent insupportable) de l'acide de départ.
- En fin de manipulation, lavez le tube à l'eau et au liquide vaisselle, ne conservez pas et ne touchez pas le contenu.
4 Explications
- Une réaction d'estérification peut avoir lieu lorsqu'un acide et un alcool sont présents dans un milieu acide (l'acide sulfurique sert de catalyseur). Le fait d'augmenter la température accélère la réaction d'estérification mais n'est pas indispensable : en chauffant avec un bec Bunsen la réaction atteint son équilibre au bout d'une minute ; à température ambiante il faudrait plusieurs semaines avant d'atteindre l'équilibre !
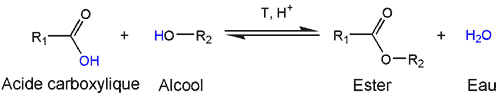
- Certains acides carboxyliques possèdent une odeur nauséabonde : c'est le cas des acides propanoïque, butanoïque, pentanoïque. Mais les esters ont une odeur agréable souvent fruitée. L'estérification étant une réaction équilibrée (non-totale) et réversible (double flèche), une petite quantité d'acide de départ est toujours présente ce qui peut masquer l'odeur de l'ester. Même un ester purifié, lorsqu'il est placé en milieu acide et en présence d'eau, peut subir une hydrolyse acide (réaction inverse de l'estérification, de la droite vers la gauche ci-dessus). On comprend alors que certaines copies bon-marchés de parfums se dégradent facilement au cours d'une journée lorsqu'on les porte sur une peau (milieu humide et acide), et peuvent donner des odeurs désagréables.
- On peut noter qu'en milieu basique il peut se produire une hydrolyse basique, et ceci de manière totale, et qui s'appelle une saponification (voir la fabrication du savon).
5 En savoir plus
Plusieurs molécules peuvent aussi rappeler une même odeur[1]. Par exemple, pour un parfum de fraise, on peut utiliser ces composés :
- benzoate de benzyle
- isobutyrate d'éthyle
- 3-méthyl-3-phénylglucidate d'éthyle
- (+/-)-3-phénylglycidate d'éthyle
- cinnamate de méthyle
- propionate de méthyle
- butyrate de phenéthyle
- isovalérate de 3-phenylpropyle
- acétate de piperonyle
- 3-methylbutanoate d'hexyle
- isobutyrate de maltyle
- 4-hydroxy-2,5-diméthyl-3(2H)-furanone (une cétone)
Dans la catégorie des odeurs fraîches mentholée on trouve :
- acétate de l-carvyle
- propionate de l-carvyle
- salicylate d'éthyle
- salicylate de méthyle (le winter green)
- acétate de 3-octyle
- l-carvéol (un alcool)
- dl-menthol (un alcool)
- l-carvone (une cétone à forte odeur de menthe)
- l-menthone (une cétone)
Certains mélanges d'esters auraient une odeur particulièrement suave et harmonieuse[2], comme celui-ci :
- cinnamate d'éthyle
- benzoate d'éthyle
- phénylacétate d'éthyle
Certaines estérifications peuvent être réalisées avec les micro-ondes. Voir l'expérience : Synthèse d'un ester par micro-ondes
Une substance peut avoir une odeur ressentie comme différente selon sa concentration. Voir : Odeur variable de l'indole
6 Références
- ↑ Catalogue Flavors & Fragrances, Aldrich (1998-1999)
- ↑ Oh, la chimie !, Paul Depovere ; Dunod (2008), 2e édition, ISBN 2-10-049497-2