Extraction de la salicyline de plantes
| Cette page fait partie des articles à relire. | |
| Si vous relevez des fautes, merci de les signaler sur la page de discussion ou les corriger directement. | |
| Pour contribuer au wiki, prenez connaissances du protocole de contribution et des règles de contribution, identifiez-vous et prenez modèle sur d'autres pages du wiki. |
Depuis l'Antiquité, l'homme connaît les vertus des infusions ou décoctions de l'écorce de Saule, de la Myrte ou encore de la Reine-des-près, contre la fièvre et les autres affections de type inflammatoire. Ici, nous allons voir comment extraire le principe actif de ces plantes et le transformer en aspirine.
Sommaire
1 Un peu d'histoire
Ce n'est qu'au 19e siècle que le principal principe actif de ces plantes -la salicyline- fut isolé par un pharmacien qui réalisa une simple décoction d’écorce de Saule blanc réduite en poudre, suivie de la filtration de la décoction et d'une concentration du filtrat ; il obtint des cristaux blancs, solubles dans l'eau qu'il baptisa salicyline (du latin salix le saule). Cette fameuse salicyline s'avéra un remède très efficace tout comme le salicylate de sodium lui aussi isolé à partir de ces plantes. Cependant les graves brûlures d'estomac provoquées par ce traitement, pourtant très efficace, représenta alors un problème majeur auquel il fallait pallier.
Ainsi, vers le milieu du 19e est synthétisé l'acide acétylsalicylique qui présente les mêmes vertus thérapeutiques que l'acide salicylique et est moins agressif pour l'estomac que le salicylate de sodium.
Finalement, le brevet et la marque de l'aspirine sont déposés par la société Bayer en 1899, sous la dénomination "Aspirin". La préparation arrive en France en 1908 et est commercialisée par la Société chimique des usines du Rhône.
L'aspirine est actuellement produite industriellement en trois étapes à partir du benzène :
- Le benzène subit une alkylation avec du propène en phase gazeuse en présence d'acide phosphorique, ce qui conduit au cumène
- Le cumène formé subit une hydroperoxydation en présence de dioxygène, sous pression,
- L'hydroperoxyde de cumyle formé est hydrolysé, conduisant au phénol et à l'acétone, qui sont séparés par distillation.
- Le phénol est carboxylé en position ortho sous forte pression de dioxyde de carbone (synthèse de Kolbe-Schmidt).
- La fonction -OH du phénol est acylée par l'anhydride acétique.
2 Protocole
Attention: Ce protocole est purement théorique pour l'instant, il faudrait donc que plusieurs volontaires fasse les critiques nécessaires et le réalisent afin de le valider
Le but de cette expérience est de réaliser une synthèse de l'aspirine à partir de plantes qui poussent près de chez vous. Certaines plantes contiennent en effet de l'acide salicylique, de la salicyline, ou d'autres dérivés, en diverses proportions :
- Saule : plante historiquement la plus utilisée pour obtenir de l'aspirine, on utilise principalement l'écorce du Saule blanc.
- Reine-des-prés : Filipendula ulmaria.
Le principe actif majeur contenu dans ces plantes est la salicyline (et non l'acide salicylique qui est également présent mais en quantité moindre).
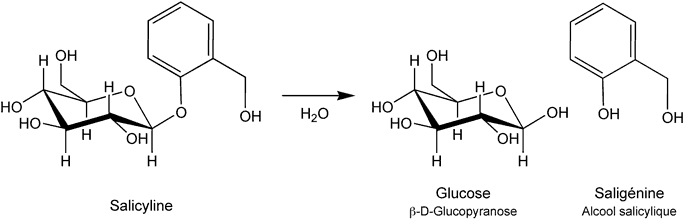
- Cette salicyline peut être hydrolysée en saligénine (2-(hydroxyméthyl)phénol) :
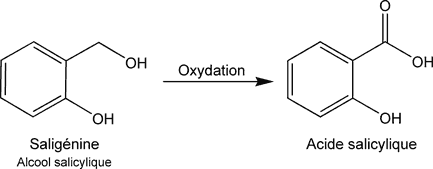
- Puis, par oxydation de la fonction alcool benzylique en acide carboxylique, on obtient l’acide salicylique :
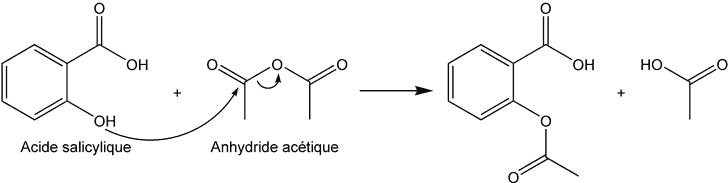
- Enfin, on acyle la fonction phénol pour obtenir l’acide acétylsalicylique.
2.1 Décoction et hydrolyse
Dans un premier temps, on réalise une décoction des extraits végétaux en milieu fortement acide afin de cliver la liaison osidique de la salicyline entre la saligénine et le glucose (cette opération peut également se faire par hydrogénation catalytique).
Si l’on veut récupérer la salicyline, sans l'hydrolyser, il ne faut pas ajouter d’acide lors de la décoction ! Au contraire, il faut utiliser de l'eau légèrement basique (pH entre 11 et 12) afin de déprotoner la fonction phénol de la salicyline ce qui la rendra encore plus hydrosoluble.
- Prendre 20 g de Reine-des-prés et les réduire en poudre fine au mortier avec de l'eau et du sable, ceci afin d’augmenter la surface de contact entre le végétal et le solvant.
- Hydrolyse de la salicyline : ajouter 50 mL d'éthanol et 10 mL d'acide chlorhydrique concentré commercial (23 à 32 %).
- Extraction de la salicyline seule : ajouter 60 mL d’eau distillée dont le pH est ajusté entre 11 et 12 par ajout de carbonate de sodium ou carbonate de potassium.
- Placer le tout dans un ballon de 250 mL et porter à reflux pendant 2h30.
- Laisser le ballon refroidir jusqu'à température ambiante.
- Filtrer sur büchner et rincer à l’éthanol. Placer le filtrat dans une ampoule à décanter de 250 mL.
- Ajouter 20 mL d'une solution d'hydroxyde de sodium pour que la solution devienne basique. L'acide salicylique est alors sous forme de salicylate de sodium soluble dans l'eau. (La saligénine aussi car un proton phénolique est acide... comment séparer l’acide salicylique de la saligénine ???)
- Introduire alors 20 mL d'acétate d'éthyle pour extraire (avec agitation et dégazage) les autres produits (comme la salicyline et la saligénine). Répéter l’opération encore deux fois. Les deux phases sont gardées.
- La phase aqueuse est réintroduite dans le ballon et on distille l’eau dans le but de concentrer la solution.
- Sous agitation lente ajouter petit à petit de l'acide chlorhydrique pour acidifier et précipiter l'acide salicylique. Filtrer sur büchner et laver les cristaux à l'eau distillée.
- La phase organique est séchée sur sulfate de sodium anhydre ou sulfate de magnésium anhydre, filtrée et concentrée à l'évaporateur rotatif. (Il conviendra d’analyser ce résidu brut pour identifier la salicyline ou la saligénine.)
2.2 Oxydation de la saligénine en acide salicylique
- Dans un ballon monocol, introduire une solution d'eau contenant 2 équivalents (molaires) de permanganate de potassium et 3 équivalents d'hydroxyde de sodium, pour un équivalent de saligénine.
- Sous agitation et à 0°C (utiliser un bain de glace), la saligénine est ajoutée goutte à goutte (éventuellement en solution dans l'eau) puis le bain de glace est retiré et le mélange est porté à reflux pendant deux heures. Il est possible de suivre la réaction par CCM si l'on a pris soin de garder un peu de saligénine en référence.
- On refroidit ensuite la solution (couleur brun foncé) dans un bain de glace et l'on filtre sur büchner pour éliminer le dioxyde de manganèse formé lors de la réaction. Le solide brun est lavé avec de l'eau froide afin de bien récupérer tout le salicylate dans le filtrat.
- Le filtrat est ensuite traité sous agitation par ajout de sulfite de sodium en poudre jusqu'à ce que la coloration violette ait disparu.
- L'acide salicylique est ensuite précipité par ajout goutte à goutte sous agitation d'acide chlorhydrique concentré dans la solution (refroidie dans un bain de glace pour diminuer la solubilité de l'acide salicylique). Les cristaux blancs sont récupérés par filtration et séchés dans un dessiccateur ou à l'étuve. Il est possible de concentrer le filtrat par évaporation de l'eau puis laisser les quelques millilitres de solution restante refroidir lentement pour former d'autres cristaux d'acide salicylique ayant échappés à la première filtration ; cependant ils seront un peu moins purs.
2.3 Acylation de l'acide salicylique en aspirine
Cette partie est déjà décrite ici : Synthèse de l'aspirine