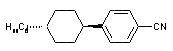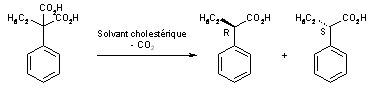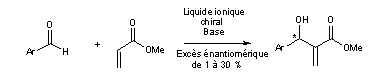Les cristaux liquides
De nos jours, sans les cristaux liquides, nous serions bien en peine ! Nos balladeurs, téléphones portables, montres à affichage numérique, certains écrans d'ordinateur, et bien d'autres objets de notre vie quotidienne, en contiennent. Voilà 120 ans qu'ils ont été découverts et ont guidé les chimistes et physiciens vers la connaissance d'un nouvel état de la matière, à mi-chemin entre le liquide et le solide cristallin.
Découvrons ici leur histoire, l'origine de leurs propriétés étranges, leurs applications et quelques exemples de synthèses.
Sommaire
1 Rapide historique
En 1888, en cherchant à déterminer la structure du cholestérol, le botaniste autrichien Reinitzer prépara le benzoate de cholestérol et observa un premier point de fusion à 145,5°C. En poussant le chauffage, il remarqua que le liquide trouble devient alors limpide à 178,5°C[1]. N’étant pas spécialiste dans l’étude des cristaux, il pris contact avec Otto Lehmann qui poursuivit l’étude des ces composés étonnant, confirma les observations de Reinitzer et inventa le premier l’appellation de cristaux liquides[2].
Mais c’est Friedel qui le premier, à partir de 1909, mena une étude cristallographique de ces composés pour mettre en évidence le caractère discontinu des transformations lors du passage d’une phase à l’autre, caractérisées de mésomorphes[3].
L’observation à l’aide d’un microscope polarisant permit de révéler certaines caractéristiques des phases et Friedel en tira les deux premières classes des cristaux liquides :
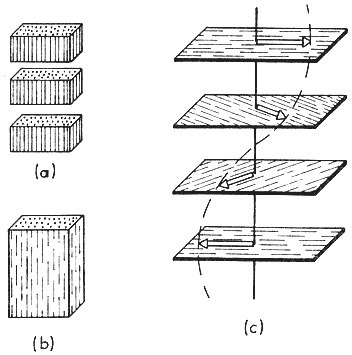
- les smectiques : constitués de molécules cylindriques formant des couches parallèles,
- les nématiques : constitués de molécules orientées dans le même sens sans répartition en couche.
Une troisième classe nommée initialement cristal liquide cholestérique, mais depuis renommé plus généralement cristal liquide nématique chiral ou hélicoïdal se rattache aux cristaux liquides nématiques.
Ces étranges molécules capables d’exister dans différentes états intermédiaires (entre solide et liquide) restèrent longtemps des curiosités de laboratoire. Mais fin 1960, la découverte de possible applications grand-public relança leur étude. Ainsi, en 1968, un chercheur de la société RCA (Radio Corporation of America) mit au point le premier afficheur à cristaux liquides où la simple application d’un champ électrique permet de modifier l’orientation des cristaux, technologie mise sur le marché cinq ans plus tard.
Pour pouvoir utiliser des cristaux liquides dans des dispositifs d’affichages, il faut que ceux-ci ne soient ni dans leur état solide ni dans leur état liquide mais dans leur état liquide nématique. Jusqu’à cette date, les cristaux liquides n’entraient dans leur phase nématique qu’à une température supérieure à la température ambiante. Puisque l’on conçoit difficilement d’utiliser une montre à 70°C, on comprend mieux l’intérêt d’un cristal liquide dans son état liquide nématique à température ambiante.
Et justement, en 1969, Kelker et Scheurle rapportèrent la préparation du premier cristal liquide présentant une phase nématique à température ambiante : le N-(4-méthoxybenzylidène)-4-butylaniline (MBBA)[4].
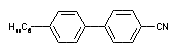
Un pas supplémentaire fut franchi quelques années plus tard par Gray et son équipe avec la préparation de cyanobiphényles nématiques à température ambiante, chimiquement et photochimiquement stables[5].
Puis en 1977, Eidenschinck mit au point des dérivés de types cyanophénylcyclohexanes, liquides nématiques à température ambiante[6].
Par la suite, les recherches s’intensifièrent avec la rationalisation du comportement des cristaux liquides et de leur développement[7][8].
Nous connaissons actuellement de nombreuses molécules dotées des propriétés des cristaux liquides :
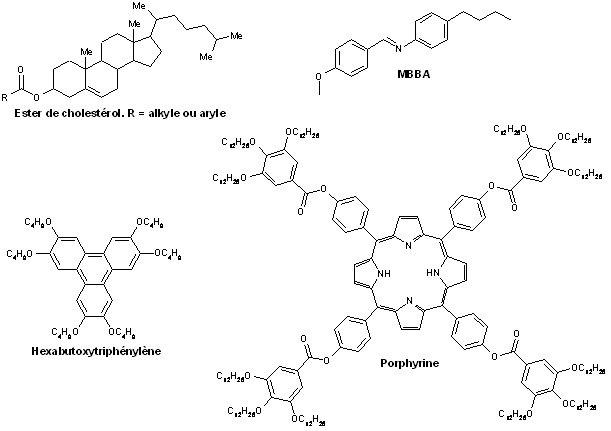
- des esters de cholestérol,
- des imines diversement fonctionnalisées (MMBA et dérivés par exemple),
- des polyaromatiques,
- des porphyrines...
Nous détaillerons par la suite la synthèse de quelques uns de ces composés.
2 Origine des étranges propriétés des cristaux liquides
Rappelons que les cristaux liquides sont caractérisés par l’existence de trois états distincts de la matière : solide, liquide nématique (souvent appelé plus simplement 'liquide cristallin') et liquide isotropique.
Passons sur l’état solide pour s’intéresser au deuxième et le plus intéressant des états : le liquide nématique ou cristallin.
Dans cet état, le composé est doté de toutes propriétés d’un liquide, prenant la forme de son contenant et formant une sphère parfaite lorsque déposé sur un liquide immiscible de même densité. Cependant, les molécules sont orientées les unes par rapport au autres, rappelant ainsi une propriété caractéristique des solides cristallins.
Le dernier état (liquide anisotropique) est un liquide classique avec une orientation aléatoire des molécules.
Avant d’aller plus loin dans la classification des cristaux liquides, nous devons dès lors préciser un terme important dans ce domaine : la partie 'mésogène'. C’est probablement la partie la plus importante du cristal liquide puisqu’elle permet d’introduire l’ordre à grande distance[9]. Ainsi, typiquement le cristal liquide est constitué d’une partie flexible (responsable de la fluidité du cristal) et d’une partie rigide appelée mésogène.
Il est possible de distinguer deux grandes classes de cristaux liquides :
- les lyotropes : formés lors du mélange de solutés (molécule amphiphile comme les tensioactifs) et de solvants dont l’un est généralement polaire,
- les thermotropes : formés par chauffage.
Dans les cristaux liquides thermotropes, plusieurs catégories existent, caractérisées par l’état de la phase liquide intermédiaire :
- smectique : les molécules sont arrangées en couches orientées parallèlement les unes aux autres. Le terme smectique a été introduit par Friedel d’après le grec σμῆγμα (savon) en raison des similitudes de réfraction de la lumière polarisée entre ces composés et une solution savonneuse.
- nématique : les molécules sont orientées dans le même sens mais sans former de strates comme précédemment. Les positions sont alors désordonnées mais les orientations ordonnées. Le terme provient encore une fois du grec νῆμα qui signifie "ligne". En effet, lorsque l’on observe ces cristaux au microscope avec de la lumière polarisée, on observe des lignes noires représentant les discontinuités entre les différentes régions de positions différentes mais de même orientation. Les cristaux liquides nématiques sont les seuls à réagir à un courant électrique. Si l’on applique une différence de potentiel entre deux électrodes enserrant un tel cristal liquide, les lignes de discontinuités vont être suffisamment larges pour bloquer la lumière, le film de cristal liquide apparaît alors opaque. C’est cette propriété, réversible, qui est utilisée dans les dispositifs d’affichage.
- nématique chiral (ou hélicoïdaux) : les molécules existent sous forme de couches parallèles les unes aux autres, les plans étant arrangés en spirale le long d’un même axe. Cet état est à l’origine d’une remarquable propriété de ce type de cristaux liquides : le changement de couleur. Ainsi certains cristaux liquides, bien qu’incolores eux-mêmes, vont réfracter la lumière les traversant d’une certaine façon et apparaître colorés. Le pas de l’hélice, tout comme la température et la pression, détermine les couleurs observées.
Les cristaux liquides formés à partir du cholestérol sont des exemples de cristaux liquides nématiques hélicoïdaux. En raison de la structure stratifiée du film de cristaux liquides, la lumière qui le traverse va être partiellement diffractée[10].
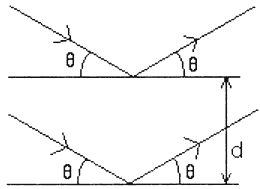
La lumière en incidence rasante va être partiellement réfléchi par une première couche. Une deuxième couche en dessous va également la réfléchir. La différence de marche δ de deux faisceaux de même longueur d'onde λ (couleur) entre les deux couches est donnée par δ = 2.d.n.sin θ, avec :
- θ : angle d’incidence du rayon lumineux
- d : distance entre deux couches (dépend du pas de l’hélice)
- n : indice de réfraction du milieu (n = 45 pour un exemple de cristal liquide).
Il y a interférence entre les deux ondes lorsque δ = p.λ, avec :
- p : un nombre entier (expérimentalement, p = 1)
- λ : longueur d’onde du rayon diffracté
On obtient alors la relation de Bragg : p.λ = 2.d.n.sin θ
La longueur d’onde du rayon diffracté (et donc la couleur de la lumière) est proportionnelle au pas de l’hélice. Toute modification du pas de l’hélice a donc bien une influence sur la couleur de la lumière.
Ainsi, les cristaux liquides cholestériques sont de bons indicateurs de température, leur couleur variant avec elle. Ils peuvent ainsi être utilisés en médecine pour réaliser des cartographies thermiques.

3 Utilisations des cristaux liquides
La toute première application des cristaux liquides a été la fabrication de dispositifs d’affichage. Et c’est dans ce domaine que ces composés se sont le plus illustrés ces dernières dizaines d’années, des montres aux écrans de télévision, ils ont envahis l’électronique grand public. C’est encore eux que l’on retrouve dans certains thermomètres changeant de couleur en fonction de la température ou encore dans des testeurs de piles...
 Rubans thermométriques réversibles.[12] |
La couleur des cristaux liquides étant capable de changer de couleur en fonction de l’angle d’observation, il est aussi possible de les rencontrer sur des billets de banque.

Certains cristaux liquides présentent d’intéressantes propriétés semiconductrices, laissant présager des applications dans le domaine de l’électronique moléculaire avec la préparation de transistors, de cellules solaires ou encore de diodes[14].
Les cristaux liquides pourraient également trouver des applications dans le domaine de stockage de données selon les nouvelles techniques holographiques[15].
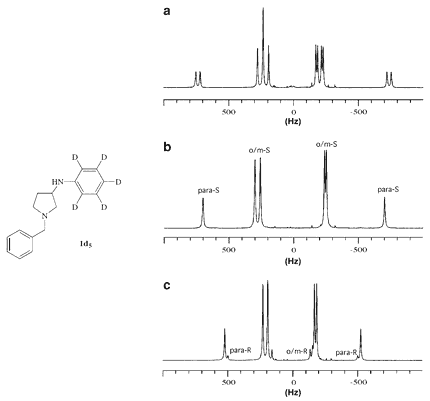
Les cristaux liquides sont également des outils de recherche comme en attestent les travaux réalisés par l’équipe des professeurs Courtieu et Merlet à l’Université d’Orsay[16]. Ces chercheurs ont en effet montrés qu’il est possible de différencier deux énantiomères d’un composé par RMN (Résonance Magnétique Nucléaire) en plaçant simplement celui-ci en solution dans un cristal liquide. Rappelons que la visualisation directe des énantiomères par RMN n’est pas possible, les deux ayant strictement le même spectre. Il faut en effet rajouter des agents de dérivation chiraux pour pouvoir les séparer (on forme alors des diastéréoisomères qui ont des spectres différents).
Les cristaux ont également été utilisés en synthèse, par exemple pour la décarboxylation énantiosélective de l’acide éthylphénylmalonique[17]. Même si l’excès énantiomérique de l’acide 2-phénylbutanoïque obtenu reste faible (18 %), il a le mérite de montrer qu’une réaction réalisée dans un solvant chiral peut se faire avec une certaine énantiosélectivité (concept repris par la suite avec des liquides ioniques chiraux[18].
4 Synthèses de cristaux liquides
Voir ces expériences :
- Synthèse des esters de cholestéryle
- Synthèse du MBBA
- Synthèse du TBBA
- Fabrication d'un affichage à cristaux liquides
5 Références
- ↑ Reinitzer F. ; Monatsh. Chem., 1888, 9, 435
- ↑ Lehmann O. ; Zeitschrift für Physikalische Chemie, 1889, 4, 462
- ↑ Friedel G. ; Ann. Physique, 1922, 18, 273
- ↑ Kelker H., Scheurle B. ; Angew. Chem. Internat. Edit., 1969, 8, 884
- ↑ Gray G.W., Harrison K.J., Nash J.A. ; Electron. Lett., 1973, 9, 130
- ↑ Eidenschink R., Erdmann D., Krause J. ; Angew. Chem. Int. Ed. Engl., 1977, 16, 100
- ↑ De Gennes P.G., Prost J. ; The physics of Liquid Cristals, 1993, Oxford University Press, London
- ↑ Kirwsch P., Bremer M. ; Angew. Chem. Int. Ed., 2000, 39, 4216
- ↑ http://en.wikipedia.org/wiki/Mesogen (en)
- ↑ Terrien M., Fournier J. ; Chimie du petit dejeuner, 1998, Cultures et techniques
- ↑ Atkins P. ; Chimie générale, 1992, InterEditions.
- ↑ http://www.tcdirect.fr/deptprod.asp?deptid=170/1
- ↑ http://www.ecb.int/euro/banknotes/html/index.fr.html
- ↑ Sergeyev S., Pisula W., Geerts Y.H. ; Chem. Soc. Rev., 2007, 36, 1902
- ↑ Matharu A.S., Jeeva S., Ramanujam P.S. ; Chem. Soc. Rev., 2007, 36, 1868
- ↑ Solgadi A., Jean L., Lasne M.C., Rouden J., Courtieu J., Meddour A. ; Tetrahedron : Assymetry, 2007, 18, 1511 – Canet I., Courtieu J., Loewenstein A., Meddour A., Pechiné J.M., J. Am. Chem. Soc., 1995, 117, 6520 – Sarfati M., Lesot P., Merlet D., Courtieu J. ; Chem. Commun., 2000, 2069 - http://www.icmmo.u-psud.fr/Labos/LRMN/
- ↑ Verbit L., Halbert T.R., Patterson R.B. ; J. Org. Chem., 1975, 40, 1649
- ↑ Pégot B., Vo-Thanh G., Gori D., Loupy A. ; Tetrahedron Letters, 2004, 45, 6425 – Nguyen Van Buu O., Vo-Thanh G. ; Letters in Organic Chemistry, 2007, 4, 158 – Pégot B., Nguyen Van Buu O., Gori D., Vo-Thanh G. ; Beilstein J. Org. Chem., 2006, 2, 18