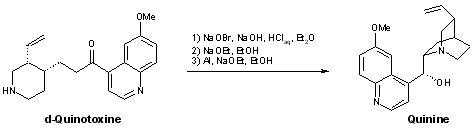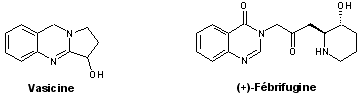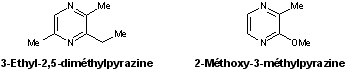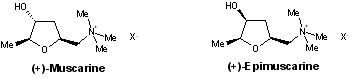Famille des alcaloïdes
Morphine, mescaline, cocaïne, strychnine, curare, codéine, caféine, théobromine, colchicine, atropine, acide lysergique... Voilà des noms de substances naturelles qui sont réputées pour leur activité biologique ! Des drogues, des excitants ou des médicaments, selon les doses et les utilisations, présents dans notre vie quotidienne, dans notre pharmacie, dans un champ de fleurs ou de blé, mais aussi dans la peau de certains animaux, pour se protéger des prédateurs. Bref, des molécules particulièrement redoutables !
Il n'est pas question ici d'apprendre à fabriquer des drogues (ce qui est formellement interdit par la loi !), mais simplement d'avoir un aperçu de leur histoire et de leur diversité moléculaire.
Sommaire
[masquer]1 Historique sur les alcaloïdes
Le terme alcaloïde (dérivé d' alcalin) rappelle qu’à l’origine ce nom avait été donné par W. Meissner, en 1819, aux substances végétales à caractère basique contenant un atome d’azote[1]. La plupart des alcaloïdes possèdent une action biologique, le plus souvent sur le système nerveux.
L’histoire des alcaloïdes débute en 1804 lorsque le chimiste allemand Paderborn découvre l’activité somnifère de l’opium. Il faudra cependant attendre 1817 pour que la communauté scientifique s’intéresse à la question avec l’isolement de la morphine contenue dans l’opium par Sertürner.
Par la suite, la strychnine puis la caféine ![]() furent découvertes respectivement en 1818 et 1819.
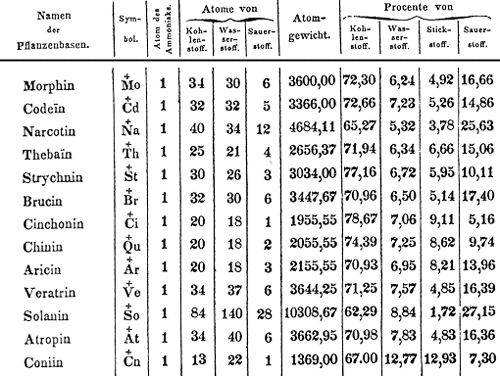
À partir de ce moment, les recherches sur l’isolement des alcaloïdes vont se développer et, en 1837, le chimiste suédois Jöns Jacob Berzelius[2], dans son dictionnaire de chimie, accorde une partie aux "sels des bases végétales" où les alcaloïdes étaient désignés sous forme de symboles[3].
furent découvertes respectivement en 1818 et 1819.
À partir de ce moment, les recherches sur l’isolement des alcaloïdes vont se développer et, en 1837, le chimiste suédois Jöns Jacob Berzelius[2], dans son dictionnaire de chimie, accorde une partie aux "sels des bases végétales" où les alcaloïdes étaient désignés sous forme de symboles[3].
À partir de 1950, les différentes techniques d’analyse (infrarouge, résonance magnétique nucléaire du proton, puis du carbone, spectrométrie de masse, etc.) feront progressivement leur entrée dans les laboratoires et permettront ainsi aux chimistes de proposer plus facilement les structures de ces substances naturelles.
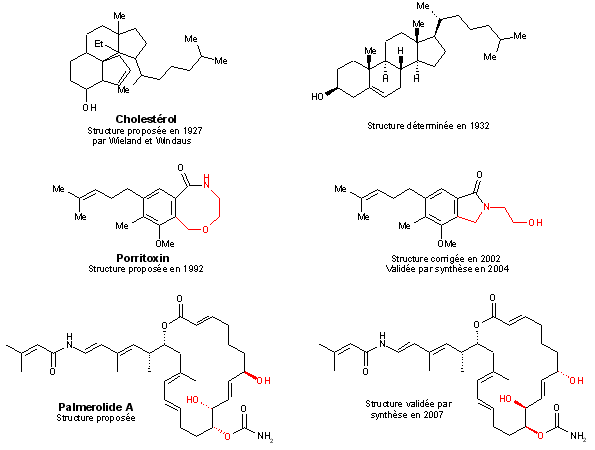
Le développement des techniques de chromatographie a également joué un rôle majeur dans l’évolution des connaissances sur le sujet, en facilitant l’isolement des composés purs. Notons toutefois qu’encore actuellement, et même en utilisant les plus récentes techniques d’analyses, on ne considère comme définitivement admise la structure d’un produit naturel qu’une fois sa synthèse achevée. L’histoire regorge d’exemples où la structure proposée (via les analyses) est différente de la structure réelle du composé et si, il y a quelques dizaines d’années, les erreurs pouvaient porter sur la structure même de la molécule, actuellement elles portent majoritairement sur des questions de stéréochimie[4][5].
D’un point de vue historique, il est généralement admis que le point culminant de la synthèse des alcaloïdes a été atteint avec la préparation de la quinine par Robert Burns Woodward en 1944[6][7]. Une découverte qui a fait couler beaucoup d’encre, encore récemment, où certains remettaient en cause certaines conclusions de Woodward[8][9][10][11]. Mais une reprise récente des dernières étapes de la synthèse de la quinine, en utilisant uniquement les techniques disponibles à l’époque, a permis d’asseoir définitivement la paternité de la synthèse totale de la quinine[12][13][14].
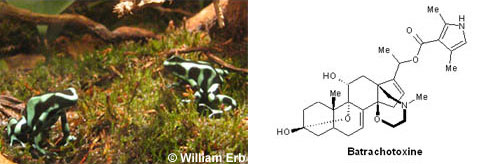
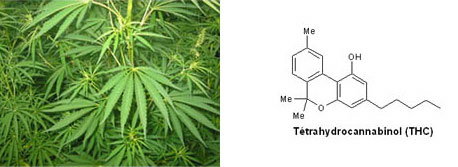
Bien que majoritairement d’origine animale, soulignons le fait que les alcaloïdes ne forment pas une famille homogène de composés chimiques mais appartient à de nombreuses familles différentes possédant structure et activité biologiques variées. L’on rattache même aujourd’hui aux alcaloïdes des composés d’origine animale telle la batrachotoxine extraite de peaux de certains batraciens ou encore le tétrahydrocannabinol (THC) extrait du cannabis d’origine végétale qui ne contient même pas d’atome d’azote.
2 Les différentes familles d’alcaloïdes
Parmi les familles des alcaloïdes, on retrouve les familles chimiques suivantes. Quelques molécules sont représentées :
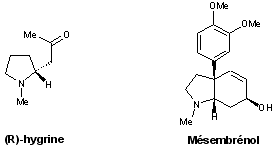
- Pyrrolidines : (R)-hygrine, mésembrenol
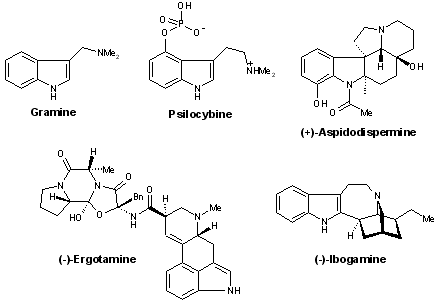
- Indoles : gramine, psilocybine, (+)-aspidospermidine, (–)-ibogamine, (–)-ergotamine
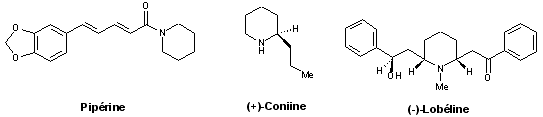
- Pipéridines : (+)-coniine, pipérine, (-)-lobéline,
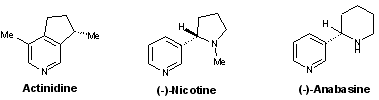
- Pyridines : actinidine, (–)-nicotine, (–)-anabasine
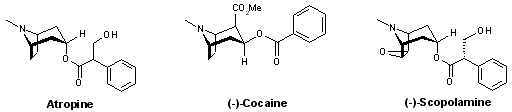
- Tropanes : (±)-atropine, (–)-cocaïne, (–)-scopolamine
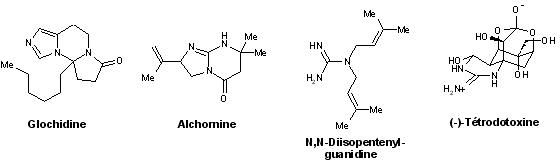
- Histamines, imidazoles et guanidines : (±)-glochidine, alchornine, N,N-diisopentenylguanidine, (–)-tétrodotoxine
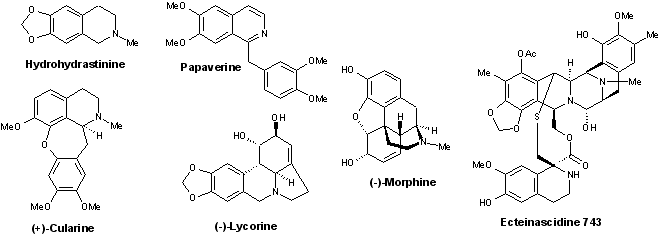
- Isoquinolines : hydrohydrastinine, papavérine, ecteinascidine 743, (+)-cularine, (–)-morphine, (–)-licorine
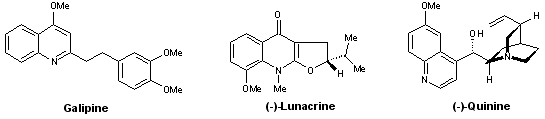
- Quinoléines : galipine, (–)-lunacrine, (–)-quinine
- Quinazolines : vasicine, (+)-fébrifugine
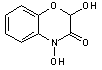
- Benzoxazines et benzoxazoles : DIBOA
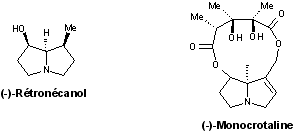
- Pyrrolozidines : (–)-rétronécanol, (–)-monocrotaline
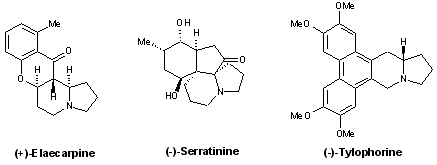
- Indolizidines : (+)-élaeocarpine, (–)-serratinine, (–)-tylophorine
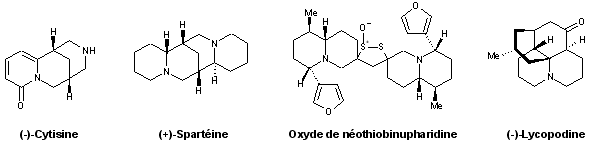
- Quinolizidines : (–)-cytisine, (–)-tinctorine, (+)-spartéine, oxyde de néothiobinupharidine, (–)-lycopodine
- Pyrazines : 3-éthyl-2,5-diméthylpyrazine, 2-méthoxy-3-méthylpyrazine
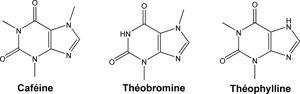
- Purines : caféine, théobromine, théophylline[16]
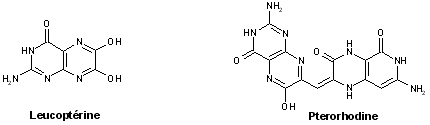
- Ptéridines : leucoptérine, ptérorhodine
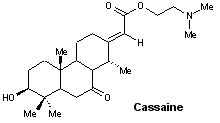
- Érythrophléums [17]
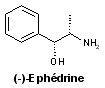
- Phénylalkylamines : (–)-éphédrine
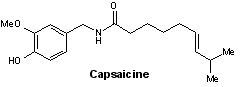
- Benzylamines : capsaïcine
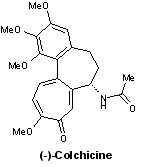
- Colchicines :
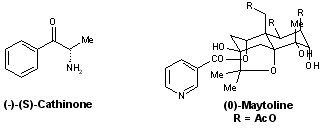
- Cathedulines : (–)-cathinone, (0)-maytoline
- Muscarines : (+)-muscarine, (+)-épimuscarine
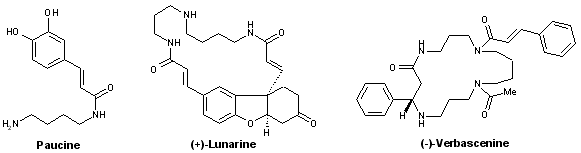
- Putrescines, spermidines et spermines : paucine, (+)-lunarine, (–)-verbascénine
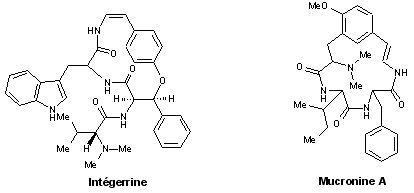
- Peptides : intégerrine, mucronine A
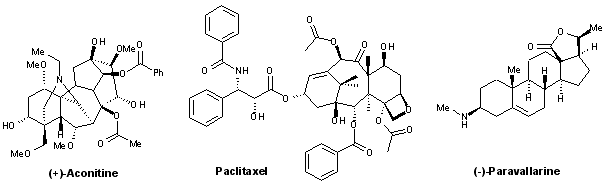
- Terpénoïdes et stéroïdes : (+)-aconitine, (–)-paclitaxel, (–)-paravallarine
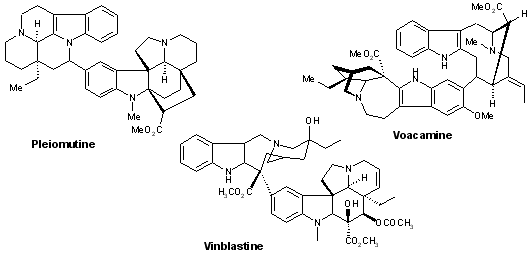
- Alcaloides dimériques : pleiomutine, voacamine, vinblastine
Comme nous pouvons le constater, de nombreuses familles de composés existent, allant de structures très simples (nicotine) à des structures très compliquées (paclitaxel), assorties d’activité biologiques variées : excitation des neurones dopaminergiques (cocaïne), hémostatique (ergotamine), analgésique (morphine), anticancéreux (ecteinascidine 743, paclitaxel), etc.
3 En savoir plus
- Voir :
4 Références
- Aller ↑ Hesse M. ; Alkaloids – Nature’s Curse or Blessing, Wiley – VCH, 2002
- Aller ↑ http://fr.wikipedia.org/wiki/Jöns_Jacob_Berzelius
- Aller ↑ Berzelius J. J. ; Lehrbuch der Chemie, vol. 6, Arnoldische Buchhandlung, 3e édition, Dresden, 1835-1841
- Aller ↑ Nicolaou K. C., Snyder S. A. ; Angew. Chem. Int. Ed., 2005, 44, 1012
- Aller ↑ Nicolaou K. C., Guduru R., Sun Y. P., Banerji B., Chen D. Y. K. ; Angew. Chem. Int. Ed., 2007, 46, 1
- Aller ↑ Woodward R. B., Doering W. E. ; J. Am. Chem. Soc., 1944, 66, 849
- Aller ↑ Woodward R. B., Doering W. E. ; J. Am. Chem. Soc., 1945, 67, 860
- Aller ↑ Stork G., Niu D., Fujimoto A., Koft E. R., Balkovec J. M., Tata J. R., Dake G. R. ; J. Am. Chem. Soc., 2001, 123, 3239
- Aller ↑ Rouhi M. ; Chem Eng. News, 2001, 79, 53
- Aller ↑ Stork G., Chem Eng. News, 2001, 79, 8
- Aller ↑ Stork G., Chem Eng. News, 2000, 78, 8
- Aller ↑ Smith A. C., Williams R. M. ; Angew. Chem. Int. Ed., 2008, 47, 1
- Aller ↑ Pour deux revues sur la synthèse de la quinine voir : Kaufman T. S., Ruveda E. A. ; Angew. Chem. Int. Ed., 2005, 44, 854 et Seeman J. I. ; Angew. Chem. Int. Ed., 2007, 46, 1378
- Aller ↑ Voir aussi : http://en.wikipedia.org/wiki/Quinine_total_synthesis
- Aller ↑ http://fr.wikipedia.org/wiki/Cannabis
- Aller ↑ Remarque : on considère souvent que ces molécules ne font pas partie des alcaloïdes en raison de son pH, mais de la famille des méthylxanthines. Il peut donc y avoir des différences selon les classifications.
- Aller ↑ Clarke R. L. ; Phytochemistry, 1971, 10, 851