Sulfate de cuivre pentahydraté
Un article du site scienceamusante.net.

|
| GHS07 |
|
| GHS05 |

|
| GHS09 |
- Formule : CuSO4,5H2O (CuSO4 lorsqu'il est anhydre)
- Autres dénominations : vitriol bleu, vitriol romain, chalcantite
- N°CAS : 7758-99-8 (pentahydraté) ; 7758-98-7 (anhydre)
- N°CE : 231-847-6
Sommaire
[masquer]1 Propriétés physiques[1]
- Masse molaire : 249,685 g/mol (pentahydraté) ; 159,62 g/mol (anhydre)
- Température de décomposition : 110°C (perte d'une partie de l'eau de cristallisation)
- Densité : 2,286
- Solubilité :
2 Classes et catégories de dangers - Étiquetage
Conforme au règlement CLP/SGH
- Toxicité aiguë par voie orale, catégorie 4
- Lésions oculaires graves/irritation oculaire, catégorie 1
- Danger pour le milieu aquatique, toxicité à court terme (aiguë), catégorie 1
- Danger pour le milieu aquatique, toxicité à long terme (chronique), catégorie 1
![]()
![]()
![]() Danger
Danger
- H302 : Nocif en cas d’ingestion.
- H318 : Provoque de graves lésions des yeux.
- H410 : Très toxique pour les organismes aquatiques, entraîne des effets néfastes à long terme.
2.1 Pentahydraté
| Voir / adapter / imprimer cette étiquette |
2.2 Anhydre
| Voir / adapter / imprimer cette étiquette |
3 Où s'en procurer ?
- Magasin de bricolage : utilisé pour le traitement anti-mousse des piscines et pierres extérieures.
- Jardinerie : utilisé pour le traitement des vignes et tomates. Attention à ne pas le confondre avec la bouillie bordelaise qui est composée de sulfate de cuivre et de chaux éteinte

 (en diverses proportions selon les recettes).
(en diverses proportions selon les recettes).
4 Pour en savoir plus
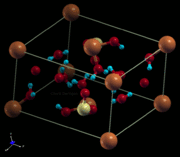
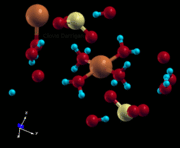
4.1 Structure cristalline
La forme cristalline de CuSO4.5H2O s'appelle la chalcantite (en anglais, chalcanthite).[2]
En connaissant les dimensions de la maille et la position des atomes dans celle-ci, on peut dessiner la maille à l'aide d'un logiciel de représentation[3].
Coordonnées utilisées pour ces figures[4] :
Groupe d'espace P-1 a = 6.141 A ; b = 10.736 ; c = 5.986 alpha = 82°16' ; beta = 107°26' ; gamma = 102°40' No x/a y/b z/c Atome 1 0.0 0.0 0.0 Cu 2 0.5 0.5 0.0 Cu 3 0.0133 0.2871 0.6253 S 4 0.9072 0.1520 0.6734 O 5 0.2442 0.3172 0.7960 O 6 0.8601 0.3724 0.6363 O 7 0.0444 0.3022 0.3849 O 8 0.8176 0.0737 0.1519 O 9 0.2887 0.1177 0.1490 O 10 0.4654 0.4063 0.2975 O 11 0.7560 0.4161 0.0191 O 12 0.4350 0.1263 0.6289 O 13 0.8980 0.1412 0.2547 H 14 0.7185 0.0126 0.2283 H 15 0.3010 0.2016 0.0667 H 16 0.3341 0.1270 0.3188 H 17 0.3231 0.3785 0.3406 H 18 0.6016 0.3937 0.4256 H 19 0.8012 0.4011 0.8847 H 20 0.8570 0.3845 0.1620 H 21 0.6033 0.1321 0.6671 H 22 0.4108 0.1932 0.6922 H
En fonction du nombre de molécules d'eau, il peut exister d'autres formes cristallines : CuSO4, CuSO4,3H2O et CuSO4,7H2O.
5 Références
- Aller ↑ CRC Handbook of Chemistry and Physics, David R. Lide, 88th edition (2007-2008). ISBN 978-0-8493-0488-0
- Aller ↑ Pour une belle photographie de ce minerais, voir : http://files.myopera.com/syracus66/albums/36620/Chalcanthite.jpg
- Aller ↑ A. Kokalj, Comp. Mater. Sci., 2003, Vol. 28, p. 155. Code available from http://www.xcrysden.org/
- Aller ↑ Zeitschrift fur Kristallographie 141 (1975) 330-341, Neutron-diffraction studies of CuSO4.5(H2O) and CuSO4.5(D2O)
- Base de donnée minéralogique, pour ceux qui veulent retrouver une structure d'après une formule ou un nom de minerais : http://rruff.geo.arizona.edu/AMS/amcsd.php (en anglais)
- Autre base de données, pointée sur la fiche de la chalcantite : http://www.mindat.org/min-959.html
- Autre base de données : http://database.iem.ac.ru/mincryst/s_carta.php?CHALCANTHITE+825</ref>